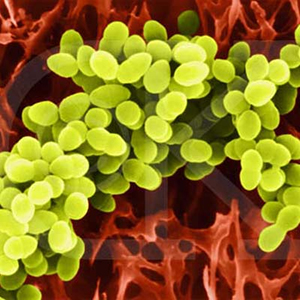
S. aureus는 사람의 비강이나 피부에서 흔히 발견되지만 특정 상황에서 심각한 감염을 일으킬 수 있는 대표적 병원균이다. 이 세균은 만성 감염과 급성 감염 모두를 통해 인체에 감염할 수 있으며, 피부와 피내 분비선 (intradermal gland)에서 화농성 감염을 일으키는 것을 포함, 호흡기, 생식기, 요도등의 점막에도 감염한다. 또한 혈관이나 림프관을 따라 퍼지면 모든 조직과 기관에서 농양이나 종기를 발생시킬 수 있는 매우 강력한 감염세균이다 (Podbielski and Kreikemeyer, 2003). 또한 병원 교차 감염 (nosocomial infection)을 매우 빈번히 일으킬 뿐만 아니라, 이러한교차 감염이 주로 강력한 메치실린 내성 S. aureus (Methicillin resistant S. aureus; MRSA)에 의해 일어나기 때문에 매우 큰 문제를 야기하는 세균이다 (Skiest et al., 2006).이 세균은 여러가지 면에서 감염에 대한 자세한 연구가 필요한 세균이다.
첫째 이유는 MRSA 와 같은 강력한 항생제 내성 때문이다. 사실 1940년대까지만 하더라도 S. aureus는 페니실린에 의해 제어가 나능했다. 첫번째 페니실린 내성 S. aureus는 1944년에 보고되었으나, 이미 1940년대 말에는 거의 50%에 달하는 S. aureus가 페니실린에 대해 내성을 보였으며, 오늘날에는 모든 S. aureus가 대부분의 페니실린 계열 항생제에 대해 저항성을 가지고 있다 (Rice, 2006). 이러한 저항성의 증가는 두 가지 기전에 의해 이루어 지는데, 여러 mobile genetic element들에 의해 내성 유전자가 수평적으로 빠르게 전파되는 것이 한가지 기전이고, 이미 존재하는 유전자에 돌연변이가 일어나는 것이 두 번째 기전이다. 이러한 저항성은 모두 항생제 처방이 시작된 1930년대 이후에 획득된 것이다 (Grundmann et al., 2006). 이중 메치실린에 대한 저항성이 가장 중요한 이유는, 메치실린 내성에 관여하는 하나의 유전 인자가 일반적으로 가장 많이 처방되는 페니실린, 세팔로스포린, 카바페넴 항생제들에 대한 내성을 부여하기 때문이다 (Grundmann et al., 2006). 최근에는 반코마이신 내성S. aureus (Vancomycin-resistant S. aureus; VRSA)에 대한 우려도 높아지고 있다 (Tenover, 2006). 이런 상황에서는 감염이 일어난 이후에 항생제로 치료하는 것은 많은 문제를 야기할 수 있다. 일단 항생제가 듣지 않을 경우가 많고, 더 많은 항생제를 쓰게 되어 더욱 강력한 내성균을 생성할 수 있기 때문이다. 따라서 감염 기전에 대한 보다 심도 있는 연구를 통해, 초기 감염을 막아서 예방하거나, 내성기전의 전파를 막으면서 감염을 치료하는 방법을 개발하는 것이 시급히 요구된다.
두번째이유는 위와 같은 필요성으로부터 S. aureus의 감염을 미연에 예방하는 방법으로 생각되어온 백신의 개발이 매우 어렵다는 점이다. 지금까지는 주로 표면 단백질이나 polysaccharide에 초점을 맞추어 왔으나, 동물실험이나 전 임상 단계의 성공에도 불구하고 실제 임상 적용에서는 모두 성공적이지 못했다 (Projan et al., 2006). 이러한 어려움의 이유로 proteinA problem과 같은 많은 가설들이 제기 되었으나 아직 명확히 이 문제를 해결하지는 못하고 있다. 따라서 초기 감염과 감염 전파에 필요한 세균 단백질에 대한 보다 심도 깊은 연구를 통해 가능성 있는 백신의 target을 개발하는 것이 매우 시급한 실정이다.
세번째이유로는 S. aureus가 매우 세련된 감염 기전을 보인다는 점이다. 이는 백신 개발이 어려운 한가지 이유이기도 한데, 감염 단계에 따라서 서로 다른 형태의 감염 단백질을 발현함으로써 자신을 변화시킨다는 점이다. 처음 표면에 부착하는 단계에서는 부착 단백질 (adhesion)을 분비해서 고착형 (sessile phenotype)을 띤다. 그러나 전파단계에서는 더 이상 adhesin을 발현하지 않고 대신 lytic 효소나 독소 (toxin)룰 분비하면서flotile 상태가 된다. 이후 제한된 구역에서 깊은 감염을 할 때는 다시 이전의 고착형 (sessile phenotype)을 발현시킨다 (Podbielski and Kreikemeyer, 2003). 이러한 변화 무쌍함으로 백신 개발을 어렵게 하는 것이다. 그러나 최근들어 이러한 상태의 변화가Quorum sensing이라는 세균의 세포간 신호전달 기전에 의해 조절된다는 것이 밝혀지면서, 이러한 Quorum signaling을 교란함에 의해 S. aureus의 변이적 감염 (metastatic infection)을 제어하려는 연구가 시도 되고 있다 (Podbielski and Kreikemeyer, 2003). 이러한 시도는, S. aureus에 의해 일어나는 골수염과 같은 만성 감염에서 매우 중요하다고 인식되고 있는 전형적인 sessile form의 하나인 biofilm 형성 또한 Quorum sensing과 관련이 된다는 결과가 나오고 있기 때문에 매우 의미가 있는 연구라 할 수 있다.